Как пишется угольная кислота. Химическая формула H2CO3 Вид молекулы Общие сведения Угольная кислота́ слабая двухосновная кислота. В чистом виде не выделена. Образуется в малых количествах. Соли угольной кислоты: классификация
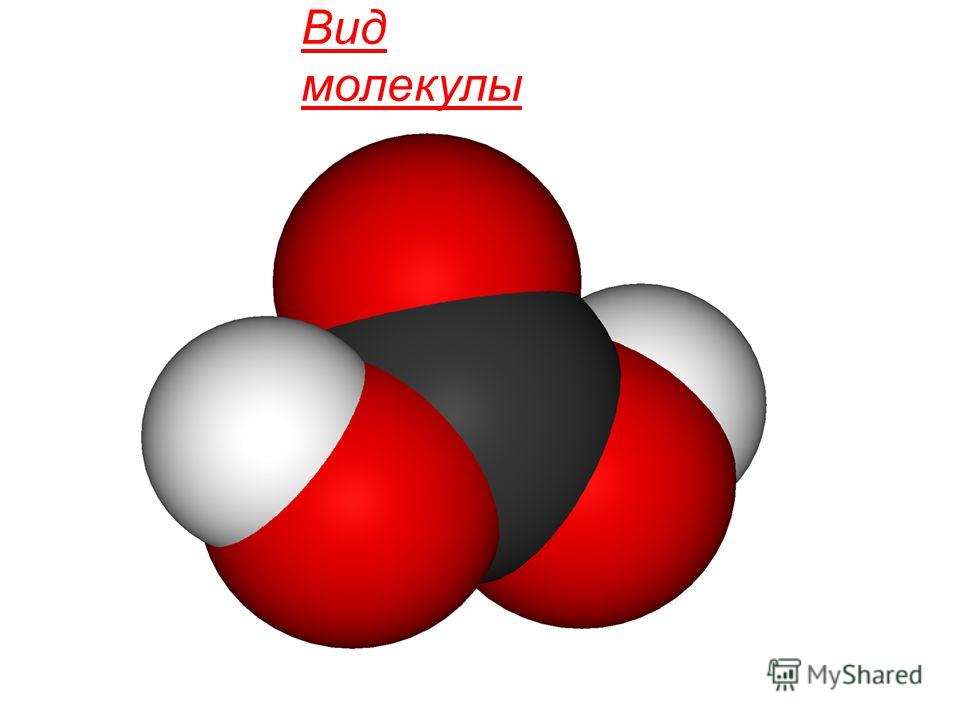

Общие сведения Угольная кислота́ слабая двухосновная кислота. В чистом виде не выделена. Образуется в малых количествах при растворении углекислого газа в воде, в том числе и углекислого газа из воздуха. Образует ряд устойчивых неорганических и органических производных: соли (карбонаты и гидрокарбонаты), сложные эфиры, амиды и др.

Это та часть, которую мы все ждали, как в мире образуется углекислота? Вы были бы потрясены, если бы обнаружили, что вам нужно только немного воды и газообразного диоксида углерода? Это, безусловно, один из способов, возможно, самый распространенный Путь, углекислота образуется. Теперь имейте в виду, что производство углекислоты в природе часто бывает спонтанным и в небольших количествах. Однако благодаря сочетанию воды и углекислого газа в атмосфере может образовываться углекислота. Это на самом деле объясняет, почему мы можем найти небольшое количество этой кислоты в дождевой воде.


Разложение При повышении температуры раствора и/или понижении парциального давления диоксида углерода равновесие в системе смещается влево, что приводит к разложению части угольной кислоты на воду и диоксид углерода. При кипении раствора угольная кислота разлагается полностью:

Следующее уравнение показывает, как карбоновая кислота образуется в результате этой реакции. Вы заметили двойные стрелки в этом уравнении? Вспомните, когда мы обсудили равновесие в отношении слабых кислот. Это прекрасный пример равновесия в действии со слабой кислотой. Существующий в равновесии угольная кислота может легко диссоциировать обратно до углекислого газа и воды. Двуокись углерода и вода могут свободно объединяться с образованием углекислоты. Это имеет смысл, поскольку в природе вещи не являются статическими.
Молекулы постоянно формируются и диссоциируются на основе таких факторов, как выветривание, атмосферные и окружающие условия. Теперь мы должны поговорить об этой концепции углекислоты, присутствующей в наших газированных напитках. Как получается, что эту слабую кислоту можно найти в нашей коке или сприте? Чтобы сделать соду, двуокись углерода должна растворяться в воде, образуя небольшие количества угольной кислоты. Эта кислота вместе с другими кислотами, такими как фосфорная кислота, дает определенную соду ее терпкий вкус.
Получение Угольная кислота образуется при растворении в воде диоксида углерода. Содержание угольной кислоты в растворе увеличивается при понижении температуры раствора и увеличении давления углекислого газа. Также угольная кислота образуется при взаимодействии её солей (карбонатов и гидрокарбонатов) с более сильной кислотой. При этом бо́льшая часть образовавшейся угольной кислоты, как правило, разлагается на воду и диоксид углерода

Кислая природа углекислоты также дает соду, которая позволяет нам свободно отрываться. Но подождите минуту, эта реакция растворения углекислого газа в воде звучит знакомо. Фактически, это тот же самый процесс, который мы обсуждали ранее в отношении присутствия углекислоты в атмосфере. Это равновесное состояние диссоциации углекислоты, выделяющей углекислый газ и воду, или сочетание углекислого газа и воды для получения углекислоты, является важной реакцией в образовании угольной кислоты. В следующий раз, когда вы жраете эту соду или поймаете, прогуливаясь сквозь ливень, подумайте о химической реакции, используемой для обеспечения присутствия углекислоты в этих источниках.
Применение Угольная кислота всегда присутствует в водных растворах углекислого газа (газированная вода). В биохимии используется свойство равновесной системы изменять давление газа пропорционально изменению содержания ионов оксония (кислотности) при постоянной температуре. Это позволяет регистрировать в реальном времени ход ферментативных реакций, протекающих с изменением pH раствора

Органические производные Угольную кислоту формально можно рассматривать как карбоновую кислоту с гидроксильной группой вместо углеводородного остатка. В этом качестве она может образовывать все производные, характерные для карбоновых кислот. Некоторые представители подобных соединений перечислены в таблице. Класс соединений Пример соединения Сложные эфиры поликарбонаты Хлорангидридыфосген Амидымочевина Нитрилыциановая кислота Ангидридыпироугольная кислота
- Манная каша на молоке: пропорции и рецепты приготовления Манная каша 1 порция
- Суп-пюре из брокколи с сыром Рецепт крем супа из брокколи с сыром
- Гороскоп: характеристика Девы, рождённой в год Петуха
- Причины выброса токсичных веществ Несгораемые углеводороды и сажа
- Современный этап развития человечества
- Лилия яковлевна амарфий Могила лилии амарфий
- Значение имени мариям Имя марьям значение происхождение

 Live Journal
Live Journal Facebook
Facebook Twitter
Twitter