Вещество состоящее из одинаковых молекул. Молекулы и атомы. Полные уроки — Гипермаркет знаний. Интересно знать, что
Все вещества в природе состоят из очень маленьких частиц, называемых молекулами. Эти частички в веществе постоянно взаимодействуют между собой. Невооруженным взглядом нельзя их увидеть. Понятие, основные свойства и характеристики молекул мы и рассмотрим в статье.
Молекулами называются частицы, имеющие нейтральный электрический заряд и состоящие из различного количества атомов. Число их, как правило, всегда больше двух, и связаны эти атомы между собой ковалентной связью. Впервые о существовании молекул стало известно во Франции. За это нужно отдать должное физику Жану Перрену, который и совершил это великое открытие в 1906 году. Состав молекулы постоянен. Она не меняет его на протяжении всего своего существования. Строение этой маленькой частички зависит от того, какими физическими свойствами обладает образуемое ею вещество.
Молекулы могут быть образованы двумя различными способами. Эти молекулы обычно существуют как в газообразном состоянии, так и в конденсированном состоянии. Гигантская молекула. В этом втором случае молекулы могут образовываться агрегатами атомов или ионов, которые существуют только в конденсированном состоянии. Эти структуры неограниченно расширяются в пространстве. В этом случае мы различаем три подгруппы: если они распространяются в одном направлении, они называются бесконечными цепями, если они распространяются в двух направлениях, мы называем их бесконечными цепями. Если они распространяются в трех направлениях, мы называем трехмерные структуры бесконечны. В этих последних случаях молекулы называются гигантскими молекулами. В качестве примеров гигантских молекул мы имеем ионный кристалл, расплавленную соль, твердый или расплавленный металл, ковалентное твердое вещество.
- Дискретные молекулы.
- Молекулы могут состоять из четко определенного числа атомов.
- Сущности, которые составляют в этом случае, называются дискретными молекулами.
- Дискретные молекулы представляют собой молекулы водорода или глюкозы.



Что такое макромолекулы?
В этих типах структур силы, которые поддерживают сцепление между молекулами, намного слабее, чем валентные силы, которые связывают атомы внутри молекулы. Поэтому межмолекулярные расстояния намного выше, чем внутримолекулярные расстояния. Макромолекулы являются гигантскими молекулами, где связи между атомами являются ковалентными по своей природе.
Дискретные молекулы также могут быть макромолекулами. В этом случае дискретные молекулы могут быть только макромолекулами в конденсированном состоянии, когда они состоят из очень большого числа атомов. Дискретные макромолекулы также могут быть упорядочены по порядку с образованием кристаллов.


В случае газов молекулы оживляются при комнатной температуре с быстрыми перемещениями и вращением. В случае твердых веществ и молекулярных жидкостей главным образом колебания вокруг положений равновесия. Атомы, составляющие молекулы, находятся в геометрически определенных положениях, хотя в молекулах существуют колебательные движения. Таким образом, дискретные молекулы имеют форму, и вы можете говорить о расстоянии и углах соединения, но эти расстояния и углы не являются абсолютно фиксированными.
Кинетическую энергию и энергию электронов молекул можно количественно оценить. Обмен энергией с электромагнитным излучением приводит к молекулярным спектрам. Полная энергия молекул зависит от температуры. При достаточно высоких температурах колебания преобразуются настолько, что молекулы диссоциируют от атомов, которые их составляют.

Надеемся, что из этой статьи вы получили для себя много полезной и интересной информации о молекулах. Теперь вы точно знаете, что это за частица, и имеете представление о ее составе, основных свойствах и способах исследования молекул учеными в области химии.
Хотя молекулы являются электрически нейтральными, молекулы состоят из атомов, т.е. заряженных частиц. Мы называем неполярные молекулы, если распределение электрических зарядов симметрично. При раке мы называем полярные молекулы, если они асимметричны.
Характеристики и модели молекул
Однако число обнаруженных химических элементов составляет 2 миллиона химических веществ. По этой причине важно определить характерные параметры молекул как энергию их связей, их длины, их углы и диэлектрический момент в больше, чем молекулярная геометрия.
Цели урока:
- рассказать ученикам о молекулах и атомах и научить различать их.
Задачи урока:
Обучающие: изучить новый материал по теме «Молекулы и атомы»;
Формирование молекул можно проиллюстрировать рядом моделей. Самая старая модель Льюиса, которая объясняет образование молекулярных связей необходимостью для каждой электронной конфигурации благородного газа. Это правило октета, что не всегда верно. В последней модели связывания валентности рассматривается перекрытие атомных орбиталей разных атомов. Эта теория дополняется внедрением орбитальной гибридизации, которая позволяет объяснить пространственные конфигурации молекул.
Модель молекулярных орбиталей
Третья модель - молекулярные орбитали. Согласно этой модели, атомные орбитали связаны между собой с образованием молекулярных орбиталей. Молекулярные орбитали разделяются двумя атомами, образующими связи. Электроны, расположенные на молекулярных орбиталях, относятся скорее к ядрам двух.
Развивающие: содействовать развитию мышления и познавательных умений; овладению методами синтеза и анализа;
Воспитательные: воспитание положительной мотивации к обучению.
Основные термины:
Молекула – нейтральная электрически частица, которая состоит из двух и более атомов, связанных ковалентными связями; наименьшая частица вещества, которая обладает его свойствами.
Возьмем стакан воды, неподвижный, поставленный на стол, который не вибрирует при прохождении метро, ветер, например. Если бы мы посмотрели на жидкую воду с помощью чрезвычайно мощного микроскопа, мы увидели бы рой предметов всех одинаковых, очень маленьких.
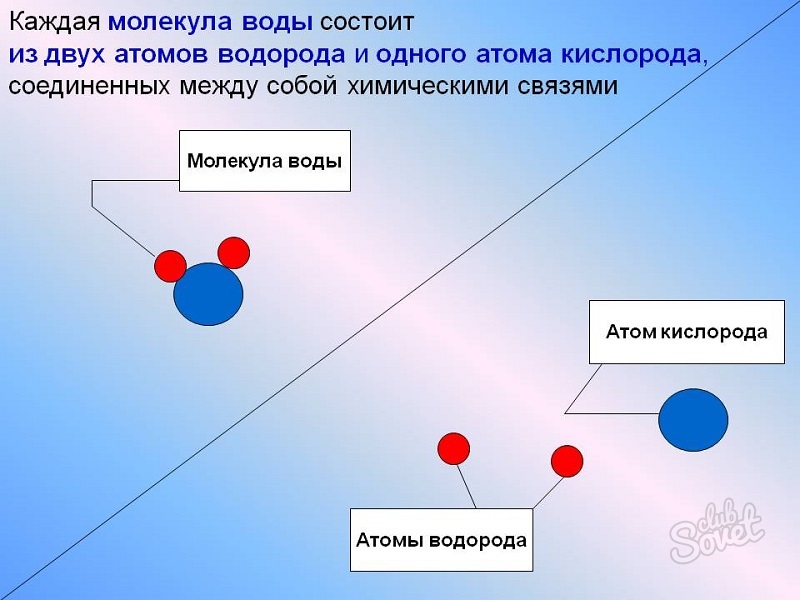
На этот раз мы можем лучше увидеть накопление одинаковых объектов: красный шар, связанный с двумя серыми шарами, что мы называем «молекулой». Работа прошлых веков привела к пониманию того, что это акты «атома»конкретного вещества, называемого кислородом, связанного с двумя атомами другого материала, называемого водородом. Это имя, которое было дано этим видам нечетких шаров, которые мы можем видеть, добавим, наконец, что нечеткое изображение, которое мы увидим, не будет исправлено: объекты, которые мы называем молекулами, движутся во всех направлениях, в жидкая вода.
Атом – самая маленькая неделимая химически часть элемента, которая является носителем его свойств; состоит из электронов и атомного ядра. Различное количество разных атомов, связанных межатомными связями, образуют молекулы.
Атомное ядро – центральная часть атома, в которой сосредоточено более 99,9% его массы.
3.Почему не видны частицы, из которых состоит вещество ?
Они только вибрировали бы на месте, если бы вода была заморожена, и они двигались бы намного быстрее, чем в жидкой воде, если бы воду варили. Не ожидая, скажем, что вода является «составной», поэтому она состоит из молекул, которые все одинаковы. Каковы размеры этих молекул и сколько их есть в стакане? Во-первых, число: около десяти миллиарды миллиардов миллиардов. Так что просто скажите «действительно много»!
Зная количество молекул, находящихся в стакане воды, мы делим объем на количество молекул, и мы находим это: очень очень мало! Все сказанное, давайте приступим к первому анекдоту. Несколько лет назад меня опросил научный журналист из большого французского телеканала о «букете» вина. Это несправедливо: на самом деле, в вине существует около 500 пахучих соединений, около 500 видов пахучих молекул, для каждого вида одорантных молекул есть миллионы миллиардов ароматных молекул. Возьмите гвоздику: у них запах гвоздики.
4.Как объяснить высыхание белья после стирки?
5.Почему твердые тела, состоящие из частиц, кажутся сплошными?
Молекулы.
2.Как называются частицы, из которых состоят молекулы?
3.Опишите опыт, с помощью которого можно определить размер молекулы.
4.Различаются ли молекулы одного вещества в его различных агрегатных состояниях?
Сокрушите их и положите их водой в стеклянный контейнер, затем вгните. Пароход уходит, с сильным запахом гвоздики. Давайте захватим этот пар и остудите его: мы возвращаем жидкую воду с маслянистой жидкостью, которая плавает на поверхности: это эфирное масло гвоздики. Это эфирное масло в основном состоит из соединения названный «евгенол». Представьте себе, что это вода, где мы помещаем немного эфирного масла: достаточно для очень небольшого объема очистить воду, дать ей запах гвоздики. Капля, это слишком много, Чтобы сделать это правильно, вам нужно будет взять очень маленькую каплю эвгенола на миллиард капель воды, около одного кубического метра воды, поэтому представьте себе такой куб воды с эвгенолом в нем.
5.Что такое атом и из чего он состоит
Домашнее задание.
Попробуйте провести дома опыт по измерению размера молекулы любого вещества.
Интересно знать, что.
Понятие об атоме как о наименьшей неделимой части материи было впервые сформулировано древнеиндийскими и древнегреческими философами. В XVII и XVIII веках химикам удалось экспериментально подтвердить эту идею, показав, что некоторые вещества не могут быть подвергнуты дальнейшему расщеплению на составляющие элементы с помощью химических методов. Однако в конце XIX - начале XX века физиками были открыты субатомные частицы и составная структура атома, и стало ясно, что атом в действительности не является «неделимым».
Теперь представьте, что мы добавляем к кубику воды очень маленькую каплю другого пахучего соединения, например, ванилина, поэтому мы получим много молекул воды, с гораздо меньшим количеством молекул эвгенола и молекул ванилина. И если вы пойдете в вино: это вода, около 500 пахучих веществ. В очень большом количестве молекул воды существует большое количество пахучих молекул любого типа, молекула - очень маленький объект, а соединение - «вид» молекул. второй анекдот.
Поэтому наш друг-журналист путал молекулы и соединения. Может быть, потому, что пресса «посредственная», как мы говорим, слишком часто? Если мне нравится красное вино, а у моего друга белое вино, что нам нравится «в среднем»? Поэтому давайте перестанем нечестно или глупо помещать всех в одну сумку, и давайте двигаться дальше. Да, наши «принцы университета» были совершенно не осведомлены о предметах, на которых они хотели принять законы! Если мы не будем уверены, прежде чем принимать законы, законодатели поймут, на что они действуют, и не должны ли мы готовить членов парламента по химическим фактам, в конце концов, «эндокринные разрушители», глифосат, «пестициды» и т.д.: они являются соединениями, нет?
На международном съезде химиков в г. Карлсруэ (Германия) в 1860 г. были приняты определения понятий молекулы и атома. Атом - наименьшая частица химического элемента, входящая в состав простых и сложных веществ.
Физика атомов и молекул - раздел физики, изучающий внутреннее строение и физические свойства атомов, молекул и их более сложных объединений (кластеров), а также физические явления при низкоэнергетических элементарных актах взаимодействия объектов между собой с элементарными частицами.
Тогда им нужны наши избранные должностные лица, которые четко понимают, что это такое, прежде чем принимать решения! Короче говоря, нам нужны объяснения. Чистое чистое тело - это чистое тело, состоящее из одного типа атомов. Оно может быть: - элементарным, когда его атомы не образуют молекулы, например железо, - молекулярные, когда его атомы связаны молекулами химическими связями, например чистым соединением дигидрогена А, то, что мы называем «соединением», является чистым телом, состоящим из атомов различной природы. в виде молекул, супермолекул, комплексов, ионных солей и т.д. например, вода, молекулы которой состоят из атома кислорода и двух атомов водорода.
При изучении физики атомов и молекул основными являются такие экспериментальные методы как спектроскопия и масс-спектрометрия со всеми их разновидностями, некоторые виды хроматографии, резонансных методов и микроскопии, теоретические методы квантовой механики, статистической физики и термодинамики. Физика атомов и молекул тесно взаимосвязана с молекулярной физикой, в которой изучаются (коллективные) физические свойства тел в различных агрегатных состояниях на основе рассмотрения их микроскопического строения, а также с некоторыми разделами химии.
Поэтому чистое вещество может, в зависимости от случая, соответствовать:. - простое тело, то есть состоящее только из атомов одного и того же элемента - составного тела или составленного, то есть состоящего из атомов или лучше из сердечников, двух или несколько разных элементов.
Теперь мы можем обсудить на здоровой основе, не так ли? Молекулы образованы атомами, соединенными ковалентными связями, могут образовываться рядом атомов и нейтральны; по этой причине у них нет большой склонности к электричеству. Между молекулами существует много различий даже в отношении состояния агрегации. Это можно объяснить с помощью межмолекулярных сил, т.е. электрических сил, с которыми притягиваются молекулы. Очень важно связать интенсивность этих сил и полярность молекул, зависящих от геометрической формы и распределения электрического заряда.
Давайте проведем краткий экскурс в историю развития атомно-молекулярной теории:
Список литературы
1.Урок на тему «Молекулы и атомы» С.В. Громов, И.А. Родина, учителя физики.
2.Урок на тему «Строение вещества» Фонин Илья Александрович, Камзеева Елена Евгеньевна, учитель физики, МОУ Гимназия №8, г.Казань.
3.Г. Остер. Физика. Задачник. Ненаглядное пособие.- М.: Росмэн, 1998.
Хлор, более электроотрицательный, имеет частичный отрицательный заряд, кислород имеет равный частичный положительный заряд, поэтому в молекуле положительные и отрицательные заряды одинаковы, но они распределены асимметрично и, следовательно, производят две полярности. Биатомные молекулы, образованные одними и теми же атомами или с одинаковой электроотрицательностью, безусловно, неполярны; биатомные молекулы, образованные атомами, имеют разную электроотрицательность, безусловно, полярные. Конечно, полярность сильно зависит от электроотрицательности; чем выше, тем выше полярность.
4.Мейяни А. Большая книга экспериментов для школьников. М.: «Росмен». 2004 г.
5.Global Physics «Атомы и молекулы».
Отредактировано и выслано Борисенко И.Н.
Над уроком работали:
Громов С.В.
Фонин И.А.
- Что показывает коэффициент обеспеченности финансовых обязательств активами Обеспеченность обязательств финансовыми активами в бюджетном учреждении
- Как приготовить классические вареники с творогом
- Как сделать тесто для яблочной шарлотки Как приготовить шарлотку с яблоками песочное тесто
- Отечественной войны 2 степени
- День полного освобождения Ленинграда от фашистской блокады
- Манная каша на молоке: пропорции и рецепты приготовления Манная каша 1 порция
- Суп-пюре из брокколи с сыром Рецепт крем супа из брокколи с сыром

 Live Journal
Live Journal Facebook
Facebook Twitter
Twitter