Простые и сложные вещества урок. Урок по химии "простые и сложные вещества". Высшую валентность азот проявляет в оксиде
Тема: Первоначальные химические представления
Урок: Развитие в науке представлений о простом и сложном веществе. Химические элементы
Вам уже знакомо имя английского исследователя Р. Бойля. Именно он предложил опыты по определению состава веществ. Рассмотрим суть таких опытов.
Чтобы установить состав вещества (проанализировать вещество) часто используют реакцию разложения, в результате которой из одного исходного вещества получается несколько продуктов реакции.
Вы когда-нибудь задумывались о том, почему некоторые вещи вызывают, пузыря, пены или меняют формы или цвета, когда вы смешиваете их вместе? Здесь вы узнаете науку за некоторыми очень крутыми реакциями - и вы даже можете попробовать их дома! Ну, ваш воздушный шар может не совсем улететь в этом эксперименте, но вы можете заставить его надуваться, создавая реакцию в бутылке.
Сделайте воронку, свернув лист бумаги в форме конуса, затем положите остроконечный конец в рот бутылки. Наденьте колпачок и встряхните бутылку, пока большая часть сахара не растворится. Снимите крышку. Поместите свою воронку в рот бутылки и вылейте дрожжи так, чтобы она плавала поверх сахарной воды. Быстро присоедините баллон к устью бутылки. Установите бутылку в место, где она не будет нарушена, и напишите в своем блокноте, в какое время оно. Вернитесь назад и проверьте бутылку через две минуты и запишите изменения, которые вы видите в жидкости в бутылке или на воздушном шаре. Проверьте его за пять минут и запишите любые изменения. Если это не похоже на то, что происходит, оставьте его примерно на 15 минут, а затем снова взгляните на него. Продолжайте проверять бутылку и баллон каждые 15 минут. Реакция может продолжаться до нескольких часов. Следите внимательно и записывайте любые изменения, которые вы замечаете!
- Вытяните воздушный шар, продувив его и выпустив воздух три раза.
- Вылейте теплую воду в бутылку.
- Вылейте сахар в бутылку через воронку.
ОПЫТ 1.
Поместим в пробирку несколько крупинок сахара и нагреем ее в пламени спиртовки. В результате прокаливания на стенках пробирки появляются капельки прозрачной жидкости, а на месте крупинок сахара образуется вещество черного цвета (Рис. 1). Если продолжать нагревание и дальше, то с черным веществом ничего не происходит. Это вещество - сажа (уголь). Его нельзя разложить ни при каких условиях.
Наиболее ярко выражены неметаллические свойства
Два вещества, дрожжи и сахар, реагировали друг на друга, и вместе они создали новое вещество - газ, называемый диоксидом углерода. Углекислый газ - это тот же газ, который делает газированную газировку, и один из многих газов в воздухе, в которые мы вдыхаем и выдыхаем. Углекислый газ из реакции заполнил все пространство в пластиковой бутылке и продолжал расти, чтобы заполнить баллон. Сначала дрожжи должны были выглядеть опухшими или пузырьками на поверхности воды, поскольку она начинала реагировать с теплом воды.
Прозрачная жидкость на стенках пробирки - это вода. Воду можно разложить на два вещества с помощью электрического тока.
Рис. 1. Разложение сахара при нагревании
Химический элемент - это разновидность атомов.
Тогда сформулируем определения простого и сложного веществ.
Простое вещество состоит из одного химического элемента (из атомов одного вида).
Тогда вы, вероятно, заметили, что воздушный шар стоял прямо вверх, вместо того, чтобы проваливаться через рот бутылки! Это был первый признак того, что дрожжи реагируют с сахаром и что углекислый газ готовят. Вскоре после этого воздушный шар должен был начать раздуваться. Поскольку воздушный шар был сделан из эластичной резины, он продолжал расширяться, чтобы удерживать углекислый газ, так же, как если бы вы взорвали его своим ртом. Когда вы выдыхаете, ваши легкие вытесняют углекислый газ вместе с несколькими другими газами, а именно, как вы можете взорвать воздушный шар.
Сложное вещество состоит из различных химических элементов (из атомов разных видов).
Важно отметить, что из одного простого вещества нельзя в ходе химической реакции получить вещество, образованное другим химическим элементом, т.к. в ходе химических реакций атомы не изменяются.
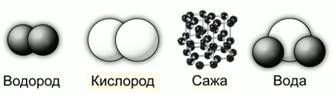
Проиллюстрируем данные определения. Молекула водорода состоит из двух атомов одного химического элемента, тоже называемого водородом. Молекула кислорода тоже состоит из двух атомов одного химического элемента, называемого кислородом. Сажа состоит только из атомов углерода. Молекула воды состоит из двух атомов водорода и одного атома кислорода, т.е. включает в себя два различных химических элемента.
Теперь, когда вы знаете, как это работает, вы можете попробовать эксперимент с другими типами сахарных смесей. Как вы думаете, что произойдет, если вы используете свою любимую соду или сок вместо сахарной воды? Итак, если дрожжи и сахар реагируют таким образом в бутылке, что происходит, когда вы печете с ними? Ну, то же самое происходит, это выглядит немного иначе. Хлеб и многие другие хлебобулочные изделия производятся из дрожжей. Дрожжи реагируют с сахаром в тесте и выделяют углекислый газ, который создает крошечные пузырьки воздуха, которые появляются и оставляют воздушные карманы, когда тесто запекает хлеб.

Рис. 4. Модели строения некоторых веществ
Названия многих химических элементов не отличаются от названий простых веществ, образованных этими элементами. Например, простое вещество водород состоит из химического элемента водорода. Простое вещество кислород состоит из химического элемента кислорода. Простое вещество железо состоит из атомов железа. Поэтому очень важно научиться различать понятия «простое вещество» и «химический элемент».
Вы можете ближе посмотреть на воздушные карманы, оставленные в куске хлеба. Белый клей Вода Пищевая окраска Стеклянная или керамическая чаша Маленькая чаша для смешивания или чашка Измерительная чашка Измерительная ложка Смешивание ложки или палочки для еды Квадрат шоколада. Вы должны увидеть большую форму скопления в цветном клеве сразу, просто продолжайте перемешивать, пока до тех пор, пока скопление не возьмет столько жидкости вокруг него, как может. Теперь придет интересная часть - отложите ложку и возьмите слизь руками. Держите его над чашей и замешивайте, как тесто, и держите его между пальцами. Когда вы будете играть с ним, слизь высохнет на ваших руках и станет менее скользкой и более похожей на шпатлевку. Держите слизь в пластиковой сумке с застежкой-молнией в холодильнике, когда вы не играете с ней.
- Хорошо перемешайте и отложите это.
- Хорошо перемешайте, пока все не смешано.
- Если вы хотите цветную слизь, добавьте 2-3 капли пищевой краситель к смеси клея.
Приведем примеры двух высказываний о кислороде, в одном из которых речь идет о химическом элементе, а в другом - о простом веществе.
Первое: «Рыбы дышат кислородом, растворенным в воде.» Второе: «В состав молекулы воды входит кислород.» Говоря о кислороде, который растворен в воде, мы имеем в виду вещество, для которого характерны определенные свойства - например, растворимость в воде.Кислород, входящий в состав молекулы воды, - это химический элемент. Т.е мы можем сказать, что атом кислорода входит в состав молекулы воды.
Высшую валентность азот проявляет в оксиде
Слово «полимер» означает «много частей». Белый клей - это один тип полимера. Этот полимер имеет свойства твердого вещества и жидкости сразу. Сравните ваш полимер с твердым предметом - кусок шоколада. Попробуйте быстро сломать пачку слизи пополам. Вы получили чистый перерыв, похожий на то, как шоколад сломался? Чтобы увидеть, как он также похож на жидкость, попробуйте медленно растянуть каплю между руками. Вы не можете сделать это с помощью твердого куска шоколада! Полимер проявляет свои жидкие свойства, когда вы растягиваете его медленно.
Есть химические элементы, которые образуют несколько различных простых веществ. Например, химический элемент углерод образует графит (тоже, что и сажа, уголь) и алмаз. Графит - нетвердое вещество серого цвета с металлическим блеском. Из него делают стержни простых карандашей.
Алмаз - минерал, имеющий самую большую твердость. Ограненный алмаз называют бриллиантом. Несмотря на то, что эти простые вещества состоят только из атомов углерода, они очень различаются по свойствам.
Теперь установите слизь обратно в миску, в которую вы вошли, и посмотрите, что произойдет. Он должен сглаживаться, чтобы заполнить нижнюю часть чаши, подобно жидкости, подобной блинчику. Каждый день вокруг нас происходят всевозможные реакции. Химическая реакция - это то, что происходит, когда два или несколько веществ вступают в контакт друг с другом. Одно вещество объединяется с другим и создает целую субстанцию, которой не было, когда началась реакция. В зависимости от веществ, которые собираются вместе, могут возникать различные типы реакций.
Свойство химического элемента, образовывать несколько простых веществ, называют аллотропией. А простые вещества, образованные одним химическим элементом, называют аллотропическими модификациями .
1. Сборник задач и упражнений по химии: 8-й класс: к учебнику П.А. Оржековского и др. «Химия, 8 класс» / П.А. Оржековский, Н.А. Титов, Ф.Ф. Гегеле. - М.: АСТ: Астрель, 2006.
Иногда после реакции возникает немного оригинальных ингредиентов, и иногда в реакции образуется несколько новых веществ. Существует также множество других химических реакций, которые происходят вокруг нас и даже внутри нас каждый день! Можете ли вы придумать какие-либо примеры? Вот несколько, чтобы вы начали.
Пищеварение - всякий раз, когда вы едите, ваше тело использует много разных и очень сложных химических реакций, чтобы разрушить пищу и превратить ее в энергию и другие вещи, которые необходимы вашему организму! Для того, чтобы существовать, для этого нужен кислород, топливо и тепло, и реакция создает свет, тепло и дым. Окисление - ржавчина - это химическая реакция, которую вы можете увидеть где-то вокруг вас. Иногда слой из красноватого цвета образуется на железе или стали, когда металл реагирует с кислородом в воздухе. Большинство железа и стали обрабатывают, чтобы предотвратить его ржавление, хотя, как правило, вы обнаруживаете ржавчину только на старых металлических изделиях, которые контактируют с большим количеством воды и постепенно ржавеют в течение нескольких лет. Когда яблоко становится коричневым после того, как вы его кусаете, это тоже окисление. Фермент во фруктовой части яблока реагирует с кислородом с воздуха и превращает яблоко в коричневый цвет. Сгорание - пожар - это еще один вид химической реакции, называемой сжиганием. . В эксперименте с шламом выше вы узнали, что такое полимер - длинная цепь из сотен или тысяч крошечных молекул.
2. Ушакова О.В. Рабочая тетрадь по химии: 8-й кл.: к учебнику П.А. Оржековского и др. «Химия. 8 класс» / О.В. Ушакова, П.И. Беспалов, П.А. Оржековский; под. ред. проф. П.А. Оржековского - М.: АСТ: Астрель: Профиздат, 2006. (с.17-19)
3. Химия: 8-й класс: учеб. для общеобр. учреждений / П.А. Оржековский, Л.М. Мещерякова, Л.С. Понтак. М.: АСТ: Астрель, 2005.(§7)
4. Химия: неорг. химия: учеб. для 8 кл. общеобр. учреждений / Г.Е. Рудзитис, ФюГю Фельдман. - М.: Просвещение, ОАО «Московские учебники», 2009. (§§5,6)
Слизь, которую вы сделали, представляет интересный тип полимера, который может действовать как твердый или жидкий в зависимости от того, как он обрабатывается. Некоторые из них естественны, а некоторые сделаны людьми или синтетическими. Вот несколько примеров полимеров. Некоторые другие вещи, происходящие из натуральных полимеров, - хлопок, шелк, резина, бумага и кожа.
- Пластмасса является одним из наиболее распространенных полимеров.
- Резина исходит из природного источника - растения!
- Прежде чем он может быть использован, он должен быть обработан.
5. Энциклопедия для детей. Том 17. Химия / Глав. ред.В.А. Володин, вед. науч. ред. И. Леенсон. - М.: Аванта+, 2003.
Дополнительные веб-ресурсы
1. Единая коллекция цифровых образовательных ресурсов ().
2. Электронная версия журнала «Химия и жизнь» ().
Домашнее задание
с. 17 №№ 4, 5 из Рабочей тетради по химии: 8-й кл.: к учебнику П.А. Оржековского и др. «Химия. 8 класс» / О.В. Ушакова, П.И. Беспалов, П.А. Оржековский; под. ред. проф. П.А. Оржековского - М.: АСТ: Астрель: Профиздат, 2006.
Химическая реакция - когда два или более веществ контактируют и образуют новое вещество. Двуокись углерода - газ, который находится в воздухе на земле, но в очень малых количествах. Растениям нужно это для того, чтобы жить; они используют его для скрытого солнечного света в пищу. Люди выдыхают углекислый газ, когда мы выдыхаем.
Кислород - газ, который очень обилен на земле и что люди и большинство животных дышат, чтобы остаться в живых. Он не имеет никакого цвета, запаха или вкуса. Полимер - слово «поли» означает много, поэтому полимер представляет собой длинную цепь молекул, которая придает веществу способность растягиваться и быть очень гибкой.
- обобщить знания по теме “Простые и сложные вещества”;
- формирование коммуникативных способностей учащихся при работе в группах.
Оборудование:
- Планшеты с меню на каждый стол – 4 шт.;
- Карта оценки вклада ученика в работу группы;
- Описание заданий (по меню) для учащихся на каждый стол – 4 шт.
- Кредит в сумме 40 у.е.
- ПСХЭ и таблица растворимости.
Учащиеся посещают кафе. Формируются 3 группы по 4 человека, каждая группа выбирает ответственного (администратора) столика. В ходе игры работа каждой группы оценивается как педагогом, так и одноклассниками (оппонентами).
Используйте этот рабочий лист как забавную деятельность, чтобы укрепить основные химические концепции химических реакций и полимеров. Дети могут покрасить страницу, а затем определить, является ли каждая фотография полимером, реакцией или нет. В этом уроке студенты различают элементы и соединения на самом базовом уровне. Студенты изучат основные характеристики элементов и соединений. В то время как студенты вводятся в молекулы и атомы в видеороликах, эти термины не изучаются в этом уроке. Избегайте ошибочного представления о том, что только соединения представлены химическими формулами.
В меню вместо обычных блюд представлены задания по теме. Каждой группе выдан кредит в сумме 40 у.е. При решении заданий учащиеся получают оценку в у.е.
Оценка деятельности учащихся производится по схеме:
“отлично” – 1 у.е., “хорошо” – 2 у.е.; “удовлетворительно” – 3 у.е.
Количество полученных у.е. вычитается из данного кредита. Победителем становится группа, сохранившая наибольшую сумму.
«Может ли золото быть изготовлено из неблагородных металлов?» Эта великая цель первых химиков, алхимиков, очаровывает по сей день. Между тем, вопросы химиков изменились, но не менее увлекательны. Какие свойства веществ можно объяснить или интерпретировать с помощью модельного мышления? Такие и подобные вопросы должны отвечать основной предметной химии. Он обеспечивает знания и навыки в отношении процессов, связанных с веществами. Студенты должны учиться правильно распознавать, наблюдать и интерпретировать, а также уменьшать сложные проблемы до простых моделей.
В ходе игры каждый участник должен выступить не менее 1 раза.
Игра проводится в несколько этапов:
1. “Холодные закуски”
- Кроссворд;
- Определение терминов;
- Распределение веществ по классам.
2. “Горячие блюда”
- Составить формулы веществ;
- Дать названия веществам;
- Решить задачу по формуле.
3. “Напитки”
Дать определение терминам
Эти вопросы необходимо уточнить на двух занятиях в неделю в течение шести семестров. Неотъемлемой частью базового обучения является стажировка, которая проводится во втором семестре и должна связать теорию с результатами экспериментов. В инструкциях основного предмета содержатся углубленные теоретические и практические знания в области химии. Он знакомит студентов с точным наблюдением, химическим мышлением, экспериментальными навыками, моделями, предметным языком и научной документацией. Показана важность основных химических исследований и многообразных применений химии в повседневной жизни и технике.
- Тест № 1.
4. “Крепкие напитки”
Тест № 2: 4 варианта.
5. “Десерт”
Отгадывание загадок.
Карта оценки вклада ученика в работу группы (проводится по 5-бальной шкале)
|
Фамилия Имя |
Оценка работы группой | Самооценка | Оценка учителя | Итоговая оценка |
Добрый день! Я рада вас приветствовать в химическом кафе “Светлячок!”. Целью работы нашего кафе будет обобщить тему “Простые и сложные вещества”. Каждый из вас занял свой столик, и я предлагаю выбрать вам администратора столика – который будет координировать работу своего столика.
Прошу вас познакомиться с меню. В нем вместо обычных блюд представлены задания по теме. Каждому нужно ответить хотя бы раз.
| Деятельность учителя | Деятельность учащихся | Химическое содержание |
| 1. Краткое сообщение о теме урока Постановка цели. Ознакомление уч-ся с правилами игры. Представление меню |
Участие в определении цели урока. Деление на группы. Выбор ответственного в группе. | |
| 2. Холодные закуски Комментарии к заданиям. Подведение результатов 1 этапа игры |
1. Кроссворд
2. Дать определение терминам:
3. Распределите следующие формулы веществ по классам: Н 2 , НС1, Na 2 SO 4 , Н 2 SO 4 , KNO 3 , ВаС1 2 , Са(ОН) 2 , Н 2 S , NaOH , О 2 , Н 2 СО 3 , N, Р, KOH , Мg СО 3 , СО 2 , Na 2 О. |
|
| 3. Горячие блюда. Комментарии к заданиям. Наблюдение за ходом работы в группах. Подведение результатов 2 этапа. | Выбор группой горячего блюда. Выполнение задания. Обсуждение в группе. Оформление на доске задания, выполненного группой. Обсуждение результатов выполнения задания. Подсчет потраченных у.е. | 1. Составить формулы веществ: N аСО 3 , Н S , Ва ОН, А1 С1, Z п S О 4 2.Дать названия следующим веществам: 3.Решите задачу: |
| 4. Напитки. Комментарии к заданиям. Наблюдение за ходом работы в группах. Подведение результатов 3 этапа. | Выполнение тренировочного тестового задания в группе. Проверка и обсуждение результатов. Выполнение тестов. Подсчет утраченных у.е. | 1. В виде простого вещества кислород содержится в
2. Высшую валентность азот проявляет в оксиде
3. Наиболее ярко выражены неметаллические свойства
4. Формулы оксида, основания, соли, соответственно:
5.Количество вещества гидроксида кальция составляет 0,25 моль. Определите его массу. |
| 5. Физкультминутка. Динамическая пауза | ||
| 6 .Крепкие напитки Комментарии к заданиям. Наблюдение за ходом работы в группах. Подведение результатов 4 этапа. | Индивидуальное выполнение тестовых заданий. Самопроверка. Заполнение теста (правильные ответы Представлены на доске) подсчет потраченных у.е. | Тест№2 - 4 варианта |
| 7
.
Десерт. Комментарии к заданиям. Подведение результатов 5 этапа.
Вручение группе победителей сладкого приза. |
Отгадывание загадок.
Подсчет остатка кредита |
1. Я, конечно, очень нужен Без меня не сваришь ужин, Не засолишь огурца, Не заправишь холодца. Но не только лишь в воде. Если льет слеза из глаза, Вкус припомнишь мой ты сразу. Кто догадлив, говорит: Это – ...(натрия хлорид) 2. Чтоб появиться
я сумел, (Диоксид углерода – углекислый газ) 3
.Горю я синим
пламенем, |
| 8. Формулировка домашнего задания | Запись домашнего задания | Составить синквейн. У кого проблемы повторить § 17– 21. |
Задания на десерт:
- Что называют белым золотом? (Хлопок. )
- Название какого химического элемента находится в супе со свеклой и другими овощами? (В– борщ. )
- Что называют “живым серебром”? (Рыбу. )
- Как называют мех пушных зверей? (Пушистое золото. )
- Выбросьте 4 букву в названии горной антилопы, и вы получите название химического элемента 6 группы. (Серна – сера. )
- С небольшого грызуна начинается, быком кончается, как химический элемент называется? (Мышьяк. )
- Какой химический элемент “зовет” к себе в гости кошку? (Кислород. )
- Манная каша на молоке: пропорции и рецепты приготовления Манная каша 1 порция
- Суп-пюре из брокколи с сыром Рецепт крем супа из брокколи с сыром
- Гороскоп: характеристика Девы, рождённой в год Петуха
- Причины выброса токсичных веществ Несгораемые углеводороды и сажа
- Современный этап развития человечества
- Лилия яковлевна амарфий Могила лилии амарфий
- Значение имени мариям Имя марьям значение происхождение

 Live Journal
Live Journal Facebook
Facebook Twitter
Twitter