Наивысшая степень окисления хлора в соединениях равна. Неорганическая химия
1. В каком соединении хлор проявляет валентность VII? 1) HClO 2) ZnCl 2 3)NaClO 3 4)HClO 4
2. Степень окисления +1 хлор проявляет в соединении 1) HClO 2) CaCl 2 3) CCl 4 4) Ca(ClO 2) 2
3. Атомы азота и углерода имеют одинаковую степень окисления в соединениях
1) NH 3 и CO 2) NO 2 и ССl 4 3) N 2 O 3 и СО 2 4) Na 3 N и CH 4
4. Высшую степень окисления хлор проявляет в соединении
Частичные уравнения должны быть умножены так, чтобы они содержали одинаковое количество электронов. В примере вы умножаете верхнее уравнение времени 2 и более низкое время. При необходимости сократите ионы кислорода. В этой реакции необходимы некоторые ионы кислорода для более низкой реакции.
Для примера реакции можно узнать из продукта, в какой среде он находится. Таким образом, три иона превращаются ионами оксония в воду. Уравнения обобщены. При желании можно добавить ионы, которые не задействованы. Пример: дихромат калия реагирует с сульфатом натрия в кислой среде.
1) KClO 2 2) KClO 4 3) СCl 4 4) MgCl 2
5. Высшую степень окисления азот имеет в соединении 1) Ca 3 N 2 2) (NH 4) 2 S 3) NO 2 4) KNO 3
6. В каком из соединений степень окисления хлора равна +7?
1) NH 4 Cl 2) KClO 3) Ca(ClO 3) 2 4) HClO 4
7. Высшую степень окисления элемент имеет в оксиде 1) N 2 O 2) Al 2 O 3 3) SO 2 4) FeO
8. Степень окисления хлора в соединении KClO 3 равна 1) –1 2) +3 3) +5 4) +7
Дихромат калия реагирует в кислой среде с сульфитом натрия с образованием хлорида хрома, хлорида калия, сульфата натрия и воды. Настроить частичные уравнения. Отрегулируйте половинные реакции. Сокращение ионов кислорода, протонов или электронов. Заполнение инертных ионов.
В окислительном состоянии -1 предпочтительно, чтобы они включали соляную кислоту и ее соли. С металлами хлор всегда образует соли, которые кристаллизуются в кристаллических решетках. Положительные состояния окисления достигаются только в соединениях фтора или кислорода.
9. В каком из соединений степень окисления фосфора равна –3?
1) K 3 Р 2) Na 3 PO 3 3) HPO 3 4)Ca 3 (PO 4) 2
10. В каком веществе степень окисления азота равна +3?
1) N 2 O 5 2) Ca 3 N 2 3) HNO 2 4) KNO 3
11. Значения высших степеней окисления элементов увеличиваются в рядах:
1) Al → P → Cl 2) Se → S → O 3) C → Si → Ge 4) Ge → As → Se 5) Be → Mg → Ca
12. Такую же степень окисления, как и в HCl, хлор имеет в соединении
Экстракция осуществляется путем добычи горной соли каменной соли, путем растворения каменной соли в течение или в течение нескольких дней и выпаривания полученного таким образом рассола или путем испарения морской воды. Для людей хлорид натрия был очень важным в течение более тысячи лет. В качестве поваренной соли, поваренной соли или просто «соли» хлорид натрия играет важную роль в питании людей с незапамятных времен. Он используется для приправы пищи, как усилителя вкуса и в качестве консерванта.
Хлорид натрия не гигроскопичен в чистом виде, увлажнение и сгущение столовой соли в воздухе связано с такими примесями. Применяется к магниевым солям. Из элементов получают хлористый водород высокой чистоты. Концентрированная соляная кислота составляет около 10 моля и имеет рН 1; Растворенная соляная кислота составляет 2 моля. Валентные электроны радикала распределены равномерно по всем трем атомам по следующим резонансным структурам.
1) Cl 2 O 2) NH 4 Cl 3) HClO 4) Cl 2 O 7
13. В каком соединении степень окисления хлора равна +7? 1) HCl 2) Cl 2 O 3) KClO 3 4) HClO 4
14. Такую же степень окисления, как и в CH 4 , углерод имеет в соединении
1) CO 2) Al 4 C 3 3) CaCO 3 4) CO 2
15. Высшую степень окисления элемент имеет в оксиде 1) CaO 2) NO 2 3) P 2 O 3 4)Cl 2 O
16. Электроотрицательность химических элементов увеличивается в ряду:
Фильтрация воды в бассейнах и водоворотах
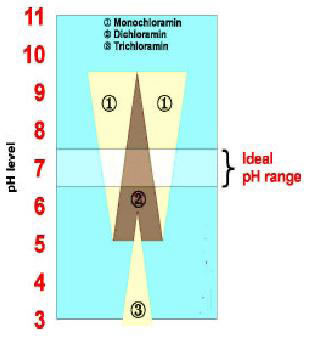
Из кислородных кислот хлора важны хлорноватистая кислота в качестве отбеливающего и дезинфицирующего агента и перхлорной кислоты. Таб. 1 Кислородные кислоты хлора. В последние годы было много исследований по трихлорамину и его потенциальному воздействию как предшественника астмы у детей или работников в бассейнах, водоворотах и спортивных центрах. Однако до сих пор мало или вообще ничего не опубликовано о том, почему образуется трихлорамин и как его производство может быть уменьшено.
У них есть способность быстро проникать в кровоток через легкие. Плавание - хорошая новость, пока качество воды и качество воздуха над поверхностью воды не вредны для вашего здоровья. В этой статье рассматривается происхождение продуктов реакции хлора и впервые с механизмом производства и представляется возможным решение проблемы. Фактически, этот подход является новаторским для всей индустрии плавательных бассейнов.
1) F → O → N 2) C → B → Be 3) Mg → Si → S 4) Be → Mg → Ca
17. Валентности элементов в водородных соединениях уменьшается в ряду
1) S → Se → Te 2) S → P → Si 3) Cl → Br → I 4) N → O → F
18. Высшую степень окисления углерод имеет в соединении 1) СО 2) СН 4 3) Na 4 C 4) Na 2 СO 3
19. Низшую степень окисления азот проявляет в соединении, формула которого
1) N 2 O 2) NO 3) NH 3 4) NCl 3

Поэтому вы всегда должны проверять коагуляцию и флокуляцию и при необходимости улучшать ее. Вторая причина высокого содержания связанного хлора может возникать при использовании чрезмерно высоких уровней свободного хлора. Поэтому крайне необходимо добавить хлор или другой окислитель только после фильтра. Решением этого является изменение местоположения добавления, уменьшение содержания хлора и улучшение линии обратной линии и частоты обратной промывки.
Высокое содержание связанного хлора, вкус трихлорамина, а также раздражение глаз у купальщиков являются признаками того, что существует проблема с водным циклом. Наиболее вероятным источником бактерий и биопленок являются песок в песчаном фильтре, активированном угольном фильтре или мертвой зоне в системе труб или в водном цикле. Согласно уравнениям реакции, трихлорамин образуется только при значениях рН ниже 5, но в правильно подготовленном плавающем бассейне рН составляет от 6, 8 до 7. Почему же могут образовываться ди - и трихлорамин?
20. Степень окисления алюминия в соединении AlCl 3 такая же, как у азота в соединении
1) NO 2) N 2 O 3 3) N 2 O 4) N 2 O 5
21. В каком соединении сера проявляет валентность VI? 1) H 2 S 2) SO 3 3) Na 2 S 4) SO 2
22. Ковалентную неполярную связь имеет каждое из двух веществ
1) C 60 и S 8 2) Na и H 2 S 3) I 2 и Ba 4) CO и KCl
23. В каком соединении степень окисления углерода равна –4?
Трихлорамин, конечно, не может образовываться непосредственно в воде, потому что рН слишком высок. Но любая поверхность, которая находится в контакте с водой в бассейне, имеет тонкую биопленку, в которой преобладает кислый рН. В этой кислотной биопленке образуется трихлорамин. Чем толще эта биопленка, тем выше образование трихлорамина.
На сегодняшний день самая большая поверхность в водовороте или бассейне имеет песчаный фильтр. Известно много лет, что песок является прекрасной почвой для роста бактерий. Свежезаваренный песок заражен различными бактериями всего за несколько дней. Бактерии выделяют так называемый «альгинат», своего рода слизь, для защиты от окислительного действия хлора. Это «соединение» может происходить всего за 30 секунд. Содержание хлора, используемое в большинстве бассейнов и водоворотов, недостаточно для того, чтобы повлиять на рост этих бактерий, защищенных альгинатом, на песке или других поверхностях.
1) CaCO 3 2) CaC 2 3) CH 4 4) NaHCO 3
24. Разную степень окисления атомы серы и углерода имеют в соединениях
1) K 2 SO 4 и CO 2 2) SO 2 и H 2 CO 3 3) Na 2 SO 3 и CO 2 4) H 2 SO 3 и CaCO 3
25. Степень окисления углерода равна –4 в соединении 1) CCl 4 2) CO 2 3) CH 4 4) CS 2
26. В каком из соединений степень окисления азота равна –3?
27. Такую же степень окисления, как и в Cl 2 O 7 , хлор имеет в соединении
Свежий песок без бактерий и песка, который через несколько дней уже показывает почти полное бактериальное заражение. На рисунке 1 показано, как чистый песок почти полностью атакован бактериями через несколько дней. Этот бактериальный слой образуется как на песке, так и на других поверхностях в бассейне. По мере развития развития биопленка становится более толстой и стабильной. В конечном итоге это приводит к тому, что альгинаты, выделяемые бактериями, вызывают склеивание зерен песка. Каналы образуют слой песка, что приводит к плохой фильтрации.
28. Значение высшей степени окисления возрастает в ряду:
1) P → S → Cl 2) Te → Se → S 3) C → Si → Ge 4) Be → B → C 5) B → Al → Ga
29. Электроотрицательность фосфора больше, чем электроотрицательность
1) хлора 2) кремния 3) азота 4) кислорода
30. Одинаковую степень окисления +5 атомы фосфора имеют в соединениях
31. Одинаковую степень окисления азот имеет в соединениях
Этот процесс обычно занимает от одного до двух лет. В сильно нагруженных системах, таких как водовороты, где бактерии имеют много органического материала в качестве источника пищи, это может произойти уже через несколько месяцев. Осаждение и прилипание песка приводят к канализации в фильтрующем слое. Это может произойти в любом фильтре. Этот клей часто называют жиром. Однако это имя неверно, потому что этот материал представляет собой бактериальную биомассу и полисахаридные альгинаты, выделяемые бактериями.
Это важно, потому что песочный фильтр является единственным механизмом, который может предотвратить распространение криптоспоридий. Если песочный фильтр имеет каналы через фильтрующий слой, криптоспоридии могут беспрепятственно проходить через фильтр.
32. Такую же степень окисления, как и в Cl 2 O 7 , хлор имеет в соединении
1) HCl 2) NH 4 ClO 4 3) Ca(ClO 3) 3 4) HClO 2
33. В каком из соединений степень окисления азота равна –3?
1) (NH 4) 2 SO 4 2) HNO 3 3) Ba(NO 2) 2 4) N 2 O 3
34. Минимальную и максимальную степень окисления атомы азота проявляют в веществах:
1) NH 3 , N 2 O 5 2) N 2 O, N 2 O 3 3) NO 2 , NO 4) NH 3 , NO
35. Такую же степень окисления, как и в Cl 2 O 7 , хлор имеет в соединении
Существует положительная корреляция между тазовой нагрузкой, количеством органического вещества, размером биопленки и образованием трихлорамина. Хорошая гигиена, правильное оборудование и дизайн очистки воды и режим работы; Важную роль играют все эти факторы.
Бактериальная биомасса в песчаном фильтре может составлять до 5% от общей массы песка. Шестнадцать из них не превзошли обычные микробиологические параметры. Поэтому бактерии могут возникать в больших количествах, даже если микробиологические тесты и тесты на безопасность являются удовлетворительными.
1) HCl 2) NH 4 ClO 4 3) Ca(ClO 3) 3 4) HClO 2
36. Одинаковую степень окисления +5 атомы фосфора имеют в соединениях
1) P 2 O 3 и PH 3 2) P 2 O 5 и H 3 PO 4 3) PH 3 и P 2 O 5 4) PH 3 и Na 3 PO 4
37. Одинаковую степень окисления азот имеет в соединениях
1) NH 3 и NO 2) NO и NO 2 3) NO 2 и N 2 O 5 4) N 2 O 5 и HNO 3
38. Одинаковую степень окисления атомы хлора имеют в соединениях:
1) Cl 2 O 7 и HClO 4 2) CaCl 2 и Mg(ClO 2) 2 3) HCl и KClO 3 4) Cl 2 O и NaClO 2
Хлор оказывает небольшое влияние, пока бактерии защищены биопленкой. Хлор может окислять те бактерии, которые вымываются из фильтра. После обратной промывки фильтра жизнеспособные бактерии могут попасть в бассейн около часа. Иногда фильтры также могут стать нестабильными, что приводит к высвобождению бактерий. Это отражается на мутности воды. В зависимости от нагрузки на фильтр это может происходить каждые несколько недель или месяцев. Хлор может убить большинство бактерий в воде в течение 30 секунд.
С бактериальными хлопьями размером от 50 до 100 мкм для их окисления требуется намного больше времени. Многие проблемы с качеством воды могут быть связаны с биопленкой, образовавшейся в песке. Правильно разработанный песочный фильтр с соответствующим процессом промывки и правильным применением будет работать хорошо. Тем не менее, песок всегда представляет определенный риск, потому что песок является отличной средой для бактерий. Поэтому мы можем категорически заключить, что даже самая тщательная обратная промывка песка не удаляет все бактерии, и поэтому песочный фильтр всегда является источником производства трихлорамина.
39. Такую же степень окисления, как и в CuS, сера имеет в соединении
1) H 2 SО 4 2) (NH 4) 2 S 3) SO 3 4) Li 2 SO 3
40. Такую же степень окисления, как и в SO 2 , сера имеет в соединении
1) K 2 SO 4 2) H 2 SO 3 3) (NH 4) 2 S 4) SO 3
41. В каком соединении углерод проявляет низшую степень окисления?
1) карбонат натрия 2) метан 3) оксид углерода (II) 4) оксид углерода (IV)
Флокуляция и питание для бактерий
Материал активно противодействует развитию бактериальных колоний, так что среднее микробное загрязнение в миллион раз меньше, чем при сопоставимом песчаном фильтре. Но это еще не все. Население удваивается примерно каждые 60 минут. Это означает, что одна бактерия может вырасти до 8 миллионов в течение 24 часов и произвести 140 кг биомассы в течение 48 часов. Очевидно, что этого не происходит с плавающими бассейнами, поскольку рост ограничен ограниченным запасом продовольствия.
Тем не менее, это объясняет, почему в высокоскоростных и горячих ваннах проблемы с фильтрами песка могут произойти через несколько месяцев. Если потребление продуктов питания снижается, рост бактерий может замедляться. Поэтому важно, чтобы посетители тщательно принимали душ перед купанием. В некоторых странах водопроводная вода также должна быть отфильтрована для удаления фосфатов и органических веществ. Ни при каких обстоятельствах поверхностно-активные вещества или моющие средства не попадают в бассейн.
42. В каком из соединений степень окисления серы равна +4?
1) K 2 SO 3 2) H 2 SO 4 3) (NH 4) 2 S 4) Fe 2 (SO 4) 3
43. Одинаковую степень окисления фосфор проявляет в каждом из двух соединений:
1) P 2 O 3 и Ca 3 P 2 2) P 4 и H 3 PO 4 3) PH 3 и H 3 PO 3 4) P 2 О 5 и H 3 PO 4
44. Высшая и низшая степени окисления углерода равны соответственно
1) +6 и –2 2) +4 и –2 3) +4 и –4 4) +6 и –4
Эффективность фильтра должна быть максимально оптимизирована для удаления максимального количества органического материала. Это может быть достигнуто путем эффективной коагуляции и флокуляции. В результате, самые твердые вещества и даже растворенные вещества могут быть отфильтрованы. Целенаправленное использование коагуляции и флокуляции уменьшает количество питательных веществ для бактерий. Это замедляет пролиферацию бактерий и уменьшает образование трихлорамина.
Известно также, что при нашей обычной концентрации хлор не способен окислять бактерии, защищенные биопленкой, - в песке, в трубах или на плитах. Когда эти питательные вещества удаляются из воды, рост бактерий прекращается. Это лишает воду фосфатов и микроэлементов и превращает их в нерастворимый осадок, который затем фильтруется фильтром.
45. Такую же степень окисления, как у хлора в Cl 2 O 5 , азот имеет в соединении
1) KNO 3 2) NO 2 3) (NH 4) 3 PO 4 4) Mg(NO 2) 2
46. В каком соединении кислород проявляет положительную степень окисления?
1) H 2 O 2 2) NO 2 3) OF 2 4) KClO 3
47. Атом кислорода проявляет степень окисления +2 в соединении
1) OF 2 2) Na 2 O 3) KOH 4) H 2 O 2
48. Отрицательную степень окисления сера проявляет в
1) Na 2 SO 3 2) (NH 4) 2 S 3) CuSO 4 4) SO 3
49. Атом серы имеет отрицательную степень окисления в соединении
1) H 2 S 2) H 2 SO 3 3) SO 2 4) Na 2 SO 4
50. Одинаковую степень окисления атомы азота имеют в соединениях N 2 O 3 и
1) Ca(NO 2) 2 2) (NH 4) 2 S 3) KNO 3 4) NH 3
Степень окисления +2 во всех соединениях проявляет
Ответ:4
Пояснение:
Из всех предложенных вариантов степень окисления +2 в сложных соединениях проявляет только цинк, являясь элементом побочной подгруппы второй группы, где максимальная степень окисления равна номеру группы.
Олово – элемент главной подгруппы IV группы, металл, проявляет степени окисления 0 (в простом веществе), +2, +4 (номер группы).
Фосфор – элемент главной подгруппы главной группы, являясь неметаллом, проявляет степени окисления от -3 (номер группы – 8) до +5 (номер группы).
Железо – металл, элемент расположен в побочной подгруппе главной группы. Для железа характерны степени окисления: 0, +2, +3, +6.
Соединение состава KЭО 4 образует каждый из двух элементов:
1) фосфор и хлор
2) фтор и марганец
3) хлор и марганец
Ответ: 3
Пояснение:
Соль состава KЭО 4 содержит кислотный остаток ЭО 4 — , где кислород обладает степенью окисления -2, следовательно, степень окисления элемента Э в этом кислотном остатке равна +7. Из предложенных вариантов подходят хлор и марганец – элементы главной и побочной подгруппы VII группы соответственно.
Фтор – также элемент главной подгруппы VII группы, однако, являясь самым электроотрицательным элементом, не проявляет положительных степеней окисления (0 и -1).
Бор, кремний и фосфор – элементы главных подгрупп 3, 4 и 5 групп соответственно, поэтому в солях проявляют соответствующие максимальные степени окисления +3, +4, +5.
Ответ: 4
Пояснение:
Одинаковую высшую степень окисления в соединениях, равную номеру группы (+5), проявляют P и As. Это элементы расположены в главной подгруппе V группы.
Zn и Cr – элементы побочных подгрупп II и VI групп соответственно. В соединениях цинк проявляет высшую степень окисления +2, хром — +6.
Fe и Mn – элементы побочных подгруппы VIII и VII групп соответственно. Высшая степень окисления у железа составляет +6, у марганца — +7.
Одинаковую высшую степень окисления в соединениях проявляют
Ответ: 4
Пояснение:
Одинаковую высшую степень окисления в соединениях, равную номеру группы (+5), проявляют P и N. Эти элементы расположены в главной подгруппе V группы.
Hg и Cr – элементы побочных подгрупп II и VI групп соответственно. В соединениях ртуть проявляет высшую степень окисления +2, хром – +6.
Si и Al − элементы главных подгруппы IV и III групп соответственно. Следовательно, для кремния максимальная степень окисления в сложных соединениях равна +4 (номер группы, где расположен кремний), для алюминия − +3 (номер группы, где расположен алюминия).
F и Mn – элементы главной и побочной подгрупп VII групп соответственно. Однако фтор, являясь самым электроотрицательным элементом Периодической системы химических элементов, не проявляет положительных степеней окисления: в сложных соединения его степень окисления равна −1 (номер группы−8). Высшая степень окисления марганца составляет +7.
Степень окисления +3 азот проявляет в каждом из двух веществ:
1) HNO 2 и NH 3
2) NH 4 Cl и N 2 О 3
Ответ: 3
Пояснение:
В азотистой кислоте HNO 2 степень окисления кислорода в кислотном остатке равна -2, у водорода — +1, следовательно, чтобы молекула оставалась электронейтральной, степень окисления азота составляет +3. В аммиаке NH 3 азот является более электроотрицательным элементом, поэтому он оттягивает на себя электронную пару ковалентной полярной связи и обладает отрицательной степенью окисления -3, степень окисления водорода в аммиаке составляет +1.
Хлорид аммония NH 4 Cl является аммонийной солью, поэтому степень окисления азота такая же, как в аммиаке, т.е. равна -3. В оксидах степень окисления кислорода всегда равна -2, поэтому у азота она составляет +3.
В нитрите натрия NaNO 2 (соли азотистой кислоты) степень окисления азота такая же, как в азота в азотистой кислоте, т.к. составляет +3. Во фториде азота степень окисления азота +3, поскольку фтор является самым электроотрицательным элементом Периодической системы и в сложных соединениях проявляет отрицательную степень окисления -1. Данный вариант ответа удовлетворяет условию задания.
В азотной кислоте азот обладает высшей степенью окисления, равной номеру группы (+5). Азот как простое соединение (поскольку состоит из атомов одного химического элемента) обладает степенью окисления 0.
Высшему оксиду элемента VI группы соответствует формула
Ответ: 4
Пояснение:
Высшим оксидом элемента является оксид элемента с его максимальной степени окисления. В группе наивысшая степень окисления элемента равна номеру группы, следовательно, в VI группе максимальная степень окисления элемента равна +6. В оксидах кислород проявляет степень окисления -2. Цифры, стоящие под символом элемента, называются индексами и указывает на количество атомов этого элемента в молекуле.
Первый вариант является неверным, т.к. элемент обладает степенью окисления 0-(-2)⋅6/4 = +3.
Во втором варианте элемент обладает степенью окисления 0-(-2) ⋅ 4 = +8.
В третьем варианте степень окисления элемента Э: 0-(-2) ⋅ 2 = +4.
В четвертом варианте степень окисления элемента Э: 0-(-2) ⋅ 3 = +6, т.е. это искомый ответ.
Степень окисления хрома в дихромате аммония (NH 4) 2 Cr 2 O 7 равна
Ответ: 1
Пояснение:
В бихромате аммония (NH 4) 2 Cr 2 O 7 в катионе аммония NH 4 + азот как более электроотрицательный элемент обладает низшей степенью окисления -3, водород заряжен положительно +1. Следовательно, весь катион обладает зарядом +1, но, поскольку этих катионов 2, то общий заряд составляет +2.
Для того чтобы молекула оставалась электронейтральной, у кислотного остатка Cr 2 O 7 2− заряд должен быть -2. Кислород в кислотных остатках кислот и солей всегда обладает зарядом -2, поэтому 7 атомов кислорода, входящих в состав молекулы бихромата аммония, заряжены -14. Атомов хрома Cr в молекулы 2, следовательно, если заряд хрома обозначить за x, то имеем:
2x + 7 ⋅ (-2) = -2, где x = +6. Заряд хрома в молекуле бихромата аммония равен +6.
Степень окисления +5 возможна для каждого из двух элементов:
1) кислорода и фосфора
2) углерода и брома
3) хлора и фосфора
Ответ: 3
Пояснение:
В первом предложенном варианте ответов только фосфор как элемент главной подгруппы V группы может проявлять степень окисления +5, которая является для него максимальной. Кислород (элемент главной подгруппы VI группы), являясь элементом с высокой электроотрицательностью, в оксидах проявляет степень окисления -2, как простое вещество – 0 и в соединении со фтором OF 2 – +1. Степень окисления +5 для него не характерна.
Углерод и бром – элементы главных подгрупп IV и VII групп соответственно. Для углерода характерна максимальная степень окисления +4 (равна номеру группы), а бром проявляет степени окисления -1, 0 (в простом соединении Br 2), +1, +3, +5 и +7.
Хлор и фосфор – элементы главных подгрупп VII и V групп соответственно. Фосфор проявляется максимальную степень окисления +5 (равную номеру группы), для хлора аналогично брому характерны степени окисления -1, 0 (в простом соединении Cl 2), +1, +3, +5, +7.
Сера и кремний – элементы главных подгрупп VI и IV групп соответственно. Сера проявляет широкий спектр степеней окисления от -2 (номер группы − 8) до +6 (номер группы). Для кремния максимальная степень окисления равна +4 (номер группы).
Ответ: 1
Пояснение:
В нитрате натрия NaNO 3 натрий имеет степень окисления +1 (элемент I группы), атомов кислорода в кислотном остатке 3, каждый из которых имеет степень окисления −2, следовательно, чтобы молекула оставалась электронейтральной, азот должен иметь степень окисления: 0 − (+1) − (−2)·3 = +5.
В нитрите натрия NaNO 2 атом натрий также имеет степень окисления +1 (элемент I группы), атомов кислорода в кислотном остатке 2, каждый из которых имеет степень окисления −2, следовательно, чтобы молекула оставалась электронейтральной, азот должен обладать степенью окисления: 0 − (+1) − (−2)·2 = +3.
NH 4 Cl − хлорид аммония. В хлоридах атомы хлора имеют степень окисления −1, атомы водорода, которого в молекуле 4, заряжен положительно, следовательно, чтобы молекула оставалась электронейтральной, степень окисления азота: 0 − (−1) − 4 ·(+1) = −3. В аммиаке и катионах аммонийных солей азот имеет минимальную степень окисления −3 (номер группы, в которой расположен элемент, − 8).
В молекуле оксида азота NO кислород проявляет минимальную степень окисления −2, как во всех оксидах, следовательно, степень окисления азота равна +2.
0EB205
Высшую степень окисления азот проявляет в соединении, формула которого
Ответ: 1
Пояснение:
Азот – элемент главной подгруппы V группы, следовательно, он может проявлять максимальную степень окисления, равную номеру группы, т.е. +5.
Одна структурная единица нитрата железа Fe(NO 3) 3 состоит из одного иона Fe 3+ и трех нитрат-ионов. В нитрат-ионах атомы азота независимо от типа противоиона имеют степень окисления +5.
В нитрите натрия NaNO 2 натрий имеет степень окисления +1 (элемент главной подгруппы I группы), атомов кислорода в кислотном остатке 2, каждый из которых имеет степень окисления −2, следовательно, чтобы молекула оставалась электронейтральной, азот должен обладать степенью окисления 0 − (+1) − (−2)⋅2 = +3.
(NH 4) 2 SO 4 – сульфат аммония. В солях серной кислоты анион SO 4 2− имеет заряд 2−, следовательно, каждый катион аммония заряжен 1+. На водороде заряд +1, поэтому на азоте −3 (азот более электроотрицателен, поэтому оттягивает на себя общую электронную пару связи N−H). В аммиаке и катионах аммонийных солей азот имеет минимальную степень окисления −3 (номер группы, в которой расположен элемент, − 8).
В молекуле оксида азота NO 2 кислород проявляет минимальную степень окисления −2, как во всех оксидах, следовательно, степень окисления азота равна +4.
28910E
В соединениях состава Fe(NO 3) 3 и CF 4 степень окисления азота и углерода равна соответственно
Ответ: 4
Пояснение:
Одна структурная единица нитрата железа (III) Fe(NO 3) 3 состоит из одного иона железа Fe 3+ и трех нитрат-ионов NO 3 − . В нитрат-ионах азот всегда имеет степень окисления +5.
Во фториде углерода CF 4 фтор является более электроотрицательным элементом и оттягивает на себя общую электронную пару связи C-F, проявляя степень окисления -1. Следовательно, углерод C имеет степень окисления +4.
A32B0B
Степень окисления +7 хлор проявляет в каждом из двух соединений:
1) Ca(OCl) 2 и Cl 2 O 7
2) KClO 3 и ClO 2
3) BaCl 2 и HClO 4
Ответ: 4
Пояснение:
В первом варианте атомы хлора обладают степенями окисления +1 и +7 соответственно. Одна структурная единица гипохлорита кальция Ca(OCl) 2 состоит из одного иона кальция Ca 2+ (Ca — элемент главной подгруппы II группы) и двух гипохлорит-ионов OCl − , каждый из которых имеет заряд 1−. В сложных соединениях, кроме OF 2 и различных перекисей, кислород всегда имеет степень окисления −2, поэтому, очевидно, что хлор имеет заряд +1. В оксиде хлора Cl 2 O 7 , как и во всех оксидах, кислород обладает степенью окисления −2, следовательно, на хлор в этом соединении имеет степень окисления +7.
В хлорате калия KClO 3 атом калия имеет степень окисления +1, а кислород — −2. Для того чтобы молекула оставалась электронейтральной, хлор должен проявлять степень окисления +5. В оксиде хлора ClO 2 кислород, как и в любом другом оксиде, обладает степенью окисления −2, следовательно, для хлора его степень окисления равна +4.
В третьем варианте катион бария в сложном соединении заряжен +2, следовательно, на каждом анионе хлора в соли BaCl 2 сосредоточен отрицательный заряд −1. В хлорной кислоте HClO 4 общий заряд 4 атомов кислорода составляет −2⋅4 = −8, на катионе водорода заряд +1. Чтобы молекула оставалась электронейтральной, заряд хлора должен составлять +7.
В четвертом варианте в молекуле перхлората магния Mg(ClO 4) 2 заряд магния +2 (во всех сложных соединениях магний проявляет степень окисления +2), поэтому на каждый анион ClO 4 − приходится заряд 1−. В общем 4 иона кислорода, где каждый проявляет степень окисления −2, заряжены −8. Следовательно, чтобы общий заряд аниона составлял 1−, на хлоре должен быть заряд +7. В оксиде хлора Cl 2 O 7 , как было объяснено выше, заряд хлора составляет +7.

 Live Journal
Live Journal Facebook
Facebook Twitter
Twitter